Дистиллят проводник тока или неэлектролит?
 Электролит – это вещество, водный раствор которого содержит частицы с разными зарядами – катионы и анионы.
Электролит – это вещество, водный раствор которого содержит частицы с разными зарядами – катионы и анионы.
Под действием электротока катионы начинают движение к катоду, а анионы – к аноду. Таким образом, вещество проводит ток.
К этой группе соединений относятся соли, кислоты и основания. Их растворы имеют высокую концентрацию заряженных частиц, которые обеспечивают проведение электротока.
Обычная неочищенная вода проводит электричество. Однако её электропроводность напрямую связана со степенью минерализации.
Чем больше солей и иных примесей растворено в ней, тем лучше проводится ток:
- электропроводность морской воды равна в среднем 30000 мкСм/см;
- у водопроводной этот показатель равен 365 мкСм/см;
- у талой или дождевой – 93 мкСм/см;
- у дистиллированной – 1-5 мкСм/см.
Приведённые показатели доказывают: дистиллированную воду нельзя считать электролитом, так как она не проводит электроток.
В процессе перегонки она практически полностью освобождается от химических примесей, способных образовывать ионы.
В чём разница?
Чем отличается дистиллированная вода от электролита? Степень электролитической диссоциации – ключевое отличие дистиллированной воды от электролита. Диссоциацией в химии называется распад молекул вещества на катионы и анионы.
Чем больше молекул распадается в растворе, тем больше степень диссоциации:
| Дистиллированная вода | Электролиты |
| 2*10-7% | Серная кислота – 60%, азотная кислота – 92%, едкий натр – 84%, поваренная соль – 84% |
Приведённые данные показывают, что молекулы электролитов при растворении почти полностью распадаются на ионы. У дистиллированной воды этот показатель настолько низкий, что им можно пренебречь.
Что лучше?
У электролита и дистиллированной воды разные функции. Вода служит растворителем и создаёт среду, в которой происходит диссоциация. Будучи свободной от посторонних примесей, она не искажает хода химической реакции и не меняет свойств диссоциирующего соединения.
Дистиллированная вода является лучшим растворителем по сравнению с другими видами H2O. Кроме того, её температура замерзания значительно ниже обычной – около -100С. Эти физико-химические свойства позволяют применять её в электротехнике.
Таким образом, вопрос о том, что лучше, некорректен. У дистиллированной воды и электролитов разные задачи. Вода нужна, чтобы получить токопроводящий раствор или уменьшить его концентрацию. Электролит добавляется в воду, чтобы повысить её электропроводность.
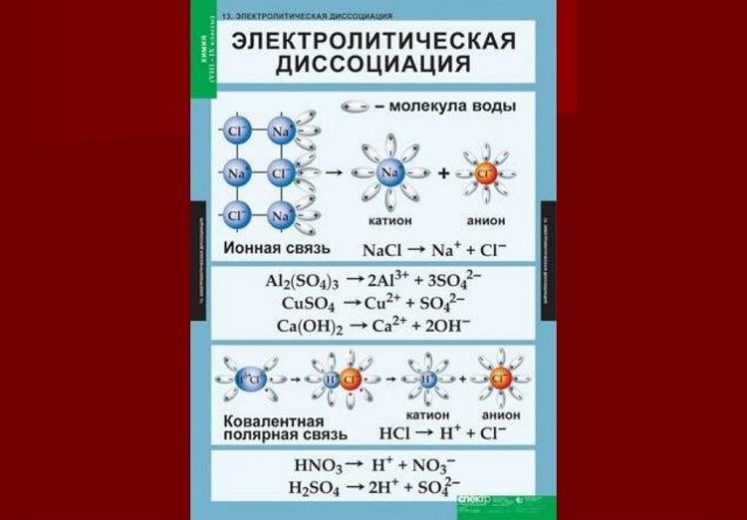 Механизм образования заряженных частиц при растворении в воде
Механизм образования заряженных частиц при растворении в воде
Можно ли смешивать?
Электролиты проявляют свои свойства только в растворах. Поэтому в технической практике их в обязательном порядке смешивают с дистиллированной водой.
Самый распространённый пример – использование в аккумуляторных кислотных батареях (АКБ) или в щелочных аккумуляторах:
- в автомобильных АКБ вода смешивается с серной кислотой;
- в щелочных аккумуляторах с едким калием или едким натром.
Чтобы аккумулятор демонстрировал хорошую ёмкость, раствор должен иметь строго определённую концентрацию. Поэтому смешивание компонентов необходимо проводить в правильных пропорциях, в соответствии с техническим регламентом.
Также стоит помнить, что при соединении кислоты и воды температура раствора повышается. Перед его использованием требуется время на остывание.
Соединяя электролит с водой, нужно концентрированное вещество понемногу добавлять в дистиллят, а не наоборот. Нарушение этого правила чревато мгновенным вскипанием раствора и химическими ожогами.
Когда используется только одно, а когда другое?
 Решение об использовании того или иного вещества принимают после замера плотности токопроводящего раствора:
Решение об использовании того или иного вещества принимают после замера плотности токопроводящего раствора:
- если концентрация слишком высока, для её уменьшения применяется чистая дистиллированная вода;
- если плотность понижена, она корректируется добавлением электролита.
Ничтожно малая электропроводность химически чистого дистиллята делает это вещество потенциальным диэлектриком. Теоретически её можно было бы заливать, например, в конденсаторы между пластинами.
Однако в реальности она не может быть идеально чистой. Поэтому в электротехнике используется только в качестве корректора плотности токопроводящего раствора.
Все, что вы хотели бы знать о дистиллированной воде, ее свойствах и применении, здесь.
Заключение
Дистиллированная вода не пропускает ток, не является электролитом, но служит необходимой средой, в которой протекают процессы электролитической диссоциации. Она используется совместно с электролитами в щелочных или кислотных аккумуляторных батареях.
Электролиты, распадаясь на ионы, пропускают через себя электроток. Однако эту способность они проявляют только при смешивании с водой.

